走进威智医药
以可靠的产品和服务,不断为客户、员工、股东、社会创造更多的价值,为更健康、更美好的生活贡献我们的才智和努力
关于威智医药
威智医药是一家以技术创新为依托,集研发、生产、服务于一体的医药健康企业,致力于满足大众日益增长的健康需求。
2006年,威智医药创立于上海,公司从研发起步,在最初的手性硼烷产品基础上不断延伸产业链。目前业务范围涵盖创新生物药、化学药品、原料药和硼烷产品四大领域。威智医药现拥有3个集成产品研发中心、3个cGMP生产基地,营销网络覆盖中国以及美国、加拿大、欧盟等国家和地区。
威智医药始终坚持以客户需求为中心,通过在医药健康领域的持续研发与创新,不断提升创新的层次、深度与广度,努力为人们提供更优质的健康产品与服务,以实际行动践行“创新为了更美好的生活”的企业使命,持续为客户、员工、股东创造价值,积极履行社会责任,为更健康、更美好的生活贡献我们的智慧与力量。

威智医药产品介绍
致力发展成为以产业链整体竞争优势为基础,以技术创新为依托的医药健康企业
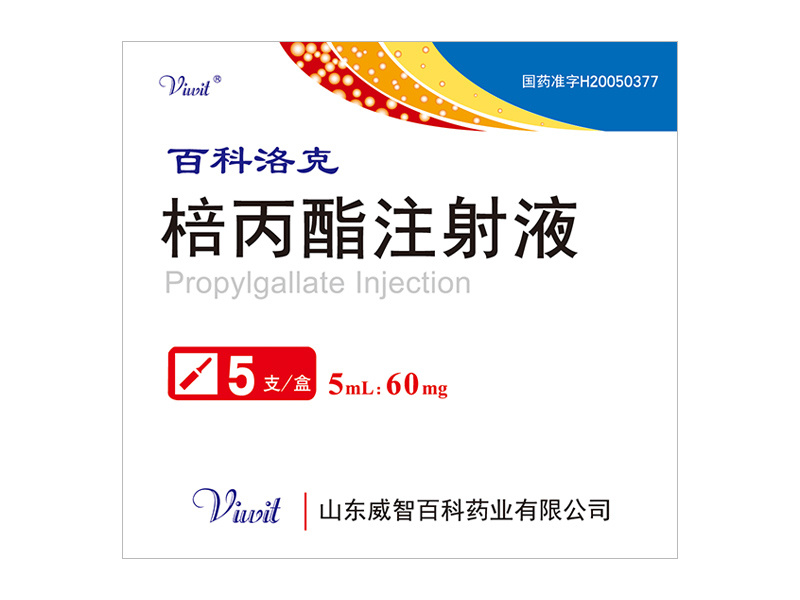
威智医药热门产品
致力发展成为以产业链整体竞争优势为基础,以技术创新为依托的医药健康企业
INNOVATION
创新创制合作平台
CDMO
提供原料药及中间体、固体口服制剂(片剂、胶囊)、无菌液体制剂(小容量注射剂-安瓿瓶、小容量注射剂-西林瓶、滴眼剂)的委托开发和生产服务(CDMO)。生产场地符合中国NMPA、美国FDA和欧盟EMA的cGMP规范。
查看更多 +
新闻资讯
在行业和社会的发展中作出应有的贡献,力图成为行业、业界的先行者。
2026
06-06
2026年6月6日,威智医药股份有限公司2025年度股东会议顺利举行。全体股东、董事及管理层齐聚一堂, 围绕公司战略、运营与治理展开高效交流,圆满完成各项议程。
2026
05-30
第39个世界无烟日|青春无烟,未来无限——科学戒烟,让健康与未来触手可及
2026年5月31日是第39个世界无烟日,今年的主题为“青春无烟,未来无限”。青少年是国家和民族的希望,而烟草正悄然侵蚀着他们的健康根基。在这个特殊的日子里,让我们共同行动起来,为青春护航,为健康发声。
2026
05-16
【省级荣誉】威智医药作品《在华十年与威智共成长》荣获2025年度山东省外国专家视频征集活动二等奖
在这个充满希望与收获的季节,一则喜讯从远方传来。近日,在由山东省国际人才交流服务中心主办的2025年度外国专家视频征集活动中,由威智医药股份有限公司精心策划推荐、外籍员工Bimal Kumar Sharma先生深度参与创作的视频作品《在华十年与威智共成长》,凭借真挚的情感与深刻的内容,从众多优秀作品中脱颖而出,荣获本次大赛二等奖!
2026
04-30
双重荣誉!魏彦君博士同时荣获滕州市及枣庄高新区“表现突出企业家”称号!
2026年4月29日,滕州市、枣庄高新区同时隆重召开2025年度高质量发展综合绩效考核总结会议。两个会议都全面总结过去一年发展成绩,通报表扬在经济社会高质量发展工作中表现突出的企业和个人,动员各级各部门和广大企业鼓足干劲、狠抓落实,为圆满完成全年目标任务凝聚奋进力量。
2026
04-24
威智医药荣获京东“创新营销奖”|总裁魏彦君博士受邀出席京东买药 10 周年暨2026京东大药房合作伙伴大会!
4月22日,威智医药总裁魏彦君博士应邀参加京东买药10周年暨2026京东大药房合作伙伴大会。在来自全国的众多医药品牌代表见证下,威智医药凭借旗下多款产品的优异疗效与过硬实力,在京东平台营销业绩位居前茅,荣获京东颁发的“创新营销奖”。

 中文
中文
 EN
EN